Комплет за екстракција и засилување на ГМО култури
Карактеристики
■ Широка применливост: Овој комплет може да извлече висококвалитетна геномска ДНК од пет главни ГМО култури.
■ Едноставно и брзо: екстракција на геномска ДНК од ГМО култури може да се заврши во рок од 2 часа. Нема потреба од големи центрифуги во фрижидер, ниски барања за инструменти и опрема. Погоден за брза геномска екстракција на ДНК на ГМО култури на сите нивоа на истражувачки институции.
■ Висока ефикасност и специфичност: Единствениот бафер на полимеразата модифицирана со антитела обезбедува ефикасно засилување на полимеразата, што е поспецифично од нормалната Taq полимераза.
Апликации
Комплетот може да извлече висококвалитетна геномска ДНК од главните ГМО култури како пченица, пченка, ориз, памук и соја, и да изврши трансгенско ПЦР откривање на ГМО култури.
Сите производи може да се прилагодат за ODM/OEM. За детали,кликнете на Приспособена услуга (ODM/OEM)
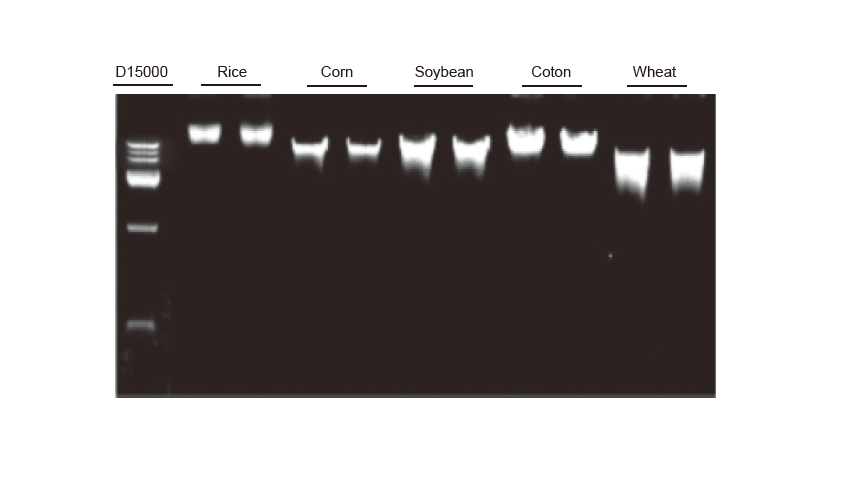 |
Геномска екстракција на ДНК Геномска екстракција на ДНК беше изведена на 100 мг лисја ориз, пченка, соја, памук и пченица, соодветно. Експериментот се повтори двапати. 3 μl ДНК од вкупните 100 μl елуенти беа вчитани по лента. Концентрацијата на гел од агароза беше 2%. Електрофорезата беше изведена под 6 V/cm 20 минути. D15000: TIANGEN D15000 ДНК маркер. |
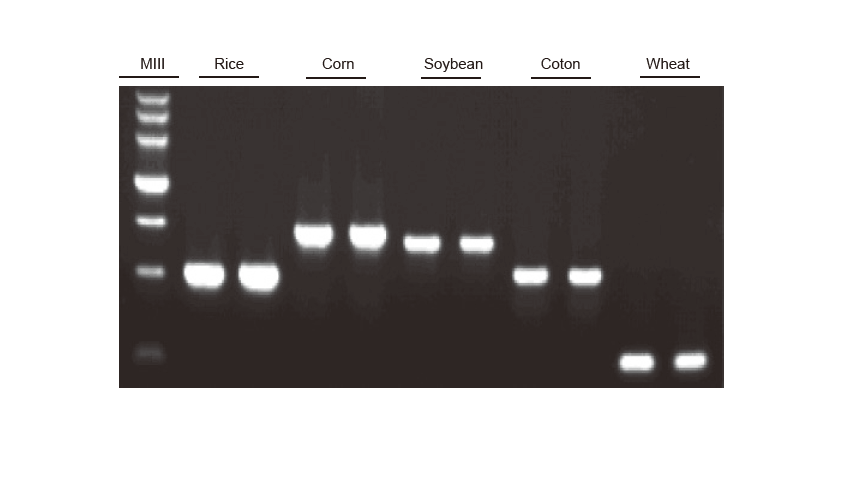 |
ПЦР Детекција Геномската ДНК на ориз, пченка, соја, памук и пченица беа соодветно засилени. Експериментот се повтори двапати. 6 μl од вкупниот 20 μl систем за реакција беа вчитани по лента. Концентрацијата на гел од агароза беше 2%. Електрофорезата беше изведена под 6 V/cm 20 минути. D15000: TIANGEN D15000 ДНК маркер. |
Шаблон А-1
■ Шаблонот содржи нечистотии од протеини или инхибитори на Taq, итн. —— Прочистете го образецот на ДНК, отстранете ги нечистотиите од протеините или извлечете ДНК на шаблонот со комплети за прочистување.
■ Денатурацијата на шаблонот не е целосна —— Соодветно зголемување на температурата на денатурација и продолжување на времето на денатурација.
Deg Деградација на шаблон-—Подгответе го образецот.
А-2 Буквар
Or Лош квалитет на прајмери-—По-синтетизирајте го прајмерот.
Deg Деградација на прајмер —— Поделете ги прајмерите со висока концентрација во мал волумен за зачувување. Избегнувајте повеќекратно замрзнување и одмрзнување или долгорочно крио-конзервирано 4 ° C.
Несоодветен дизајн на прајмери (на пр. Должината на прајмерот не е доволна, димер формиран помеѓу прајмерите итн.)
А-3 мг2+концентрација
■ Мег2+ концентрацијата е премногу ниска —— Правилно зголемување на Mg2+ концентрација: Оптимизирајте го Mg2+ концентрација со серија реакции од 1 mM до 3 mM со интервал од 0,5 mM за да се одреди оптималниот Mg2+ концентрација за секој образец и прајмер.
А-4 Температура на огревање
■ Високата температура на печење влијае врз врзувањето на прајмерот и шаблонот. - Намалете ја температурата на огнот и оптимизирајте ја состојбата со градиент од 2 ° C.
А-5 Време на продолжување
■ Кратко време на продолжување —— Зголемете го времето на продолжување.
Феномени: Негативните примероци исто така ги покажуваат опсезите на целната секвенца.
А-1 Контаминација на ПЦР
■ Вкрстена контаминација на целната секвенца или производи за засилување —— Внимателно да не го пипетирате примерокот што содржи целна секвенца во негативниот примерок или да не го истурите од цевката за центрифуга. Реагенсите или опремата треба да бидат автоклавирани за да се елиминираат постојните нуклеински киселини, а постоењето на контаминација треба да се утврди преку негативни контролни експерименти.
Контаминација со реагенс —— Активирајте ги реагенсите и чувајте ги на ниска температура.
А-2 премиерr
■ Мег2+ концентрацијата е премногу ниска —— Правилно зголемување на Mg2+ концентрација: Оптимизирајте го Mg2+ концентрација со серија реакции од 1 mM до 3 mM со интервал од 0,5 mM за да се одреди оптималниот Mg2+ концентрација за секој образец и прајмер.
Неправилен дизајн на прајмер, а целната секвенца има хомологија со нишантната секвенца. —— Редизајнирани буквари.
Феномени: Лентите за засилување на ПЦР се неконзистентни со очекуваната големина, големи или мали, или понекогаш се појавуваат и специфични појаси за засилување и неспецифични појаси.
А-1 Буквар
■ Лоша специфичност на прајмерот
--— Буквар за повторно дизајнирање.
Concentration Концентрацијата на прајмерот е премногу висока —— Правилно зголемување на температурата на денатурација и продолжување на времето на денатурација.
А-2 мг2+ концентрација
■ На Mg2+ концентрацијата е превисока —— Правилно намалете ја концентрацијата на Mg2+: Оптимизирајте го Mg2+ концентрација со серија реакции од 1 mM до 3 mM со интервал од 0,5 mM за да се одреди оптималниот Mg2+ концентрација за секој образец и прајмер.
А-3 Термостабилна полимераза
■ Прекумерна количина ензим —— Намалете ја количината на ензим соодветно во интервали од 0,5 У.
А-4 Температура на огревање
Temperature Температурата на загревање е премногу ниска-—соодветно зголемете ја температурата на огнување или усвојте го двостепениот метод на загревање
Циклуси А-5 ПЦР
■ Премногу PCR циклуси —— Намалете го бројот на PCR циклуси.
А-1 Буквар—— Лоша специфичност —— Редизајнирајте го прајмерот, сменете ја положбата и должината на прајмерот за да ја подобрите неговата специфичност; или изведете вгнездени ПЦР.
Шаблон ДНК А-2
- Шаблонот не е чист - Прочистете го образецот или извлечете ДНК со комплети за прочистување.
А-3 мг2+ концентрација
- —Мг2+ концентрацијата е превисока —— Правилно намалување на Mg2+ концентрација: Оптимизирајте го Mg2+ концентрација со серија реакции од 1 mM до 3 mM со интервал од 0,5 mM за да се одреди оптималниот Mg2+ концентрација за секој образец и прајмер.
А-4 dNTP
- Концентрацијата на dNTP е превисока - соодветно намалете ја концентрацијата на dNTP
А-5 Температура на огнување
—— Премногу ниска температура на огнување —— Соодветно зголемување на температурата на огнување
Циклуси А-6
—— Премногу циклуси —— Оптимизирајте го бројот на циклусот

Првиот чекор е да се избере соодветна полимераза. Редовната Taq полимераза не може да се лекторира поради недостаток на активност на 3'-5 'егзонуклеаза, а несовпаѓањето во голема мера ќе ја намали ефикасноста на продолжувањето на фрагментите. Затоа, редовната Taq полимераза не може ефикасно да ги засили целните фрагменти поголеми од 5 kb. Taq полимеразата со специјална модификација или друга полимераза со голема верност треба да се избере за да се подобри ефикасноста на продолжувањето и да се задоволат потребите за долго засилување на фрагменти. Покрај тоа, засилување на долги фрагменти, исто така, бара соодветно прилагодување на дизајнот на прајмер, време на денатурација, време на продолжување, тампон pH вредност, итн. Обично, прајмерите со 18-24 п.п. може да доведат до подобар принос. Со цел да се спречи оштетување на шаблонот, времето на денатурација на 94 ° C треба да се намали на 30 секунди или помалку по циклус, а времето за покачување на температурата на 94 ° C пред засилување треба да биде помало од 1 мин. Покрај тоа, поставувањето на температурата за продолжување на околу 68 ° C и дизајнирањето на времето на продолжување според стапката од 1 kb/min може да обезбеди ефикасно засилување на долги фрагменти.
Стапката на грешка при засилување на ПЦР може да се намали со употреба на разни ДНК полимерази со голема верност. Меѓу сите пронајдени досега полимерази на Taq DNA, Pfu ензимот има најниска стапка на грешка и најголема верност (видете ја приложената табела). Покрај селекцијата на ензими, истражувачите можат дополнително да ја намалат стапката на мутација на ПЦР со оптимизирање на условите на реакција, вклучувајќи оптимизирање на тампон составот, концентрација на термостабилна полимераза и оптимизирање на бројот на циклусот на ПЦР.
Категории на производи
ЗОШТО НЕ ИЗБЕРЕМЕ
Од своето основање, нашата фабрика развива производи од прва светска класа со почитување на принципот
со квалитет прво. Нашите производи се здобија со одлична репутација во индустријата и вредна доверба меѓу новите и старите клиенти.








